Service
サービスご利用の流れ
ご契約までの流れ

① お問い合せ
「iPS細胞作製・保管」及び
「リバースエイジング医療※」
を選択

② ご契約
ご契約の合意締結

③ お振込み
ご入金の確認
ご契約後の流れ

適性確認について
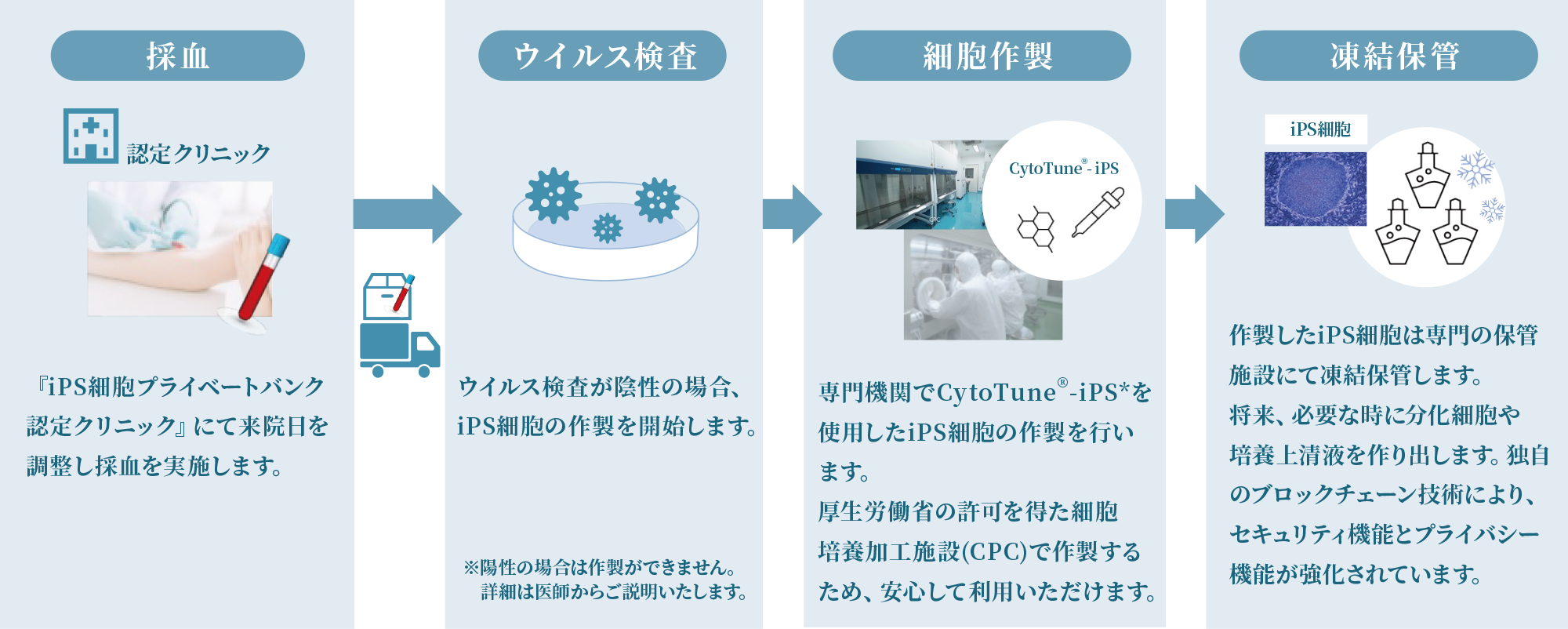
採血実施クリニックにてウイルス検査による検査をクリアした血液は、専門機関へ輸送され、細胞加工フェーズに進みます。
以下の除外基準に該当する方、またウイルス検査にて除外基準に該当すると判断された場合は、不適格と判断され、血液を廃棄する必要があります。
以下の除外基準に該当する方、またウイルス検査にて除外基準に該当すると判断された場合は、不適格と判断され、血液を廃棄する必要があります。
- ■ 結果が判定困難(陽性の疑いあり)の場合は、ご本人に結果をご説明の上、同意いただいた場合、さらに精密な確定検査を行います。
除外基準
<1> 以下の1つ以上の検査結果が
陽性の場合
- ○ B型肝炎
- ○ C型肝炎
- ○ ヒト免疫不全ウイルス(HIV-1及びHIV-2)
- ○ 成人T細胞白血病(HTLV-1)
<2> 以下の疾患を現在罹患している方
- ○ 確認、未確認の如何に関わらず、伝達性海綿状脳症
医師により判断を行う事項
<1> 告知する義務を有す疾患及び状態
- ○ 梅毒、クラミジア感染症、淋病、結核、マラリア、バベシア病、シャーガス病、リーシュマニア症、アフリカトリパノソーマ症等の菌による感染性疾患
- ○ 妊娠中、授乳中、又は妊娠している可能性のある女性
- ○ 各種がん
<2> その他
- ○ iPS細胞の製造及び使用に支障をきたすおそれのある他の疾患
- ○ その他、担当医師がiPS細胞の作製に不適当と判断した方
iPS細胞の作製
輸送された血液をもとにCytoTune®-iPSキットを用いてiPS細胞等の作製を行います。
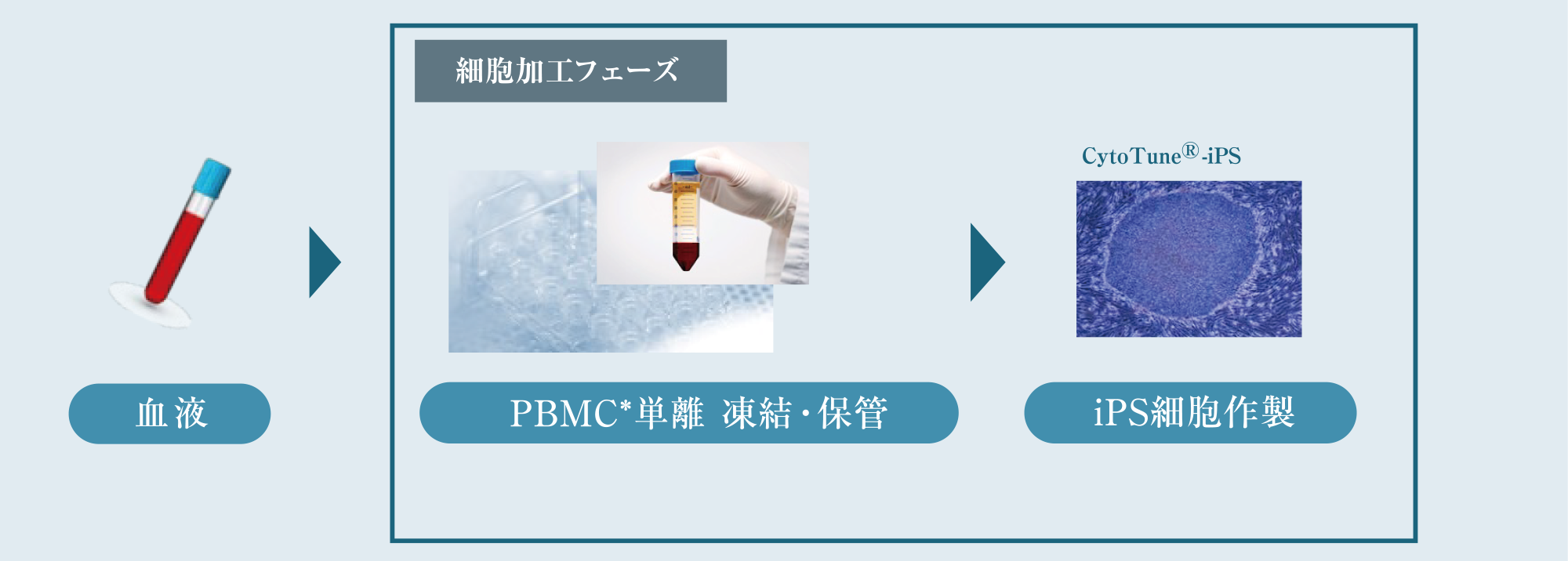
PBMCにはT細胞、B細胞、NK細胞、樹状細胞などのリンパ球が含まれます。
CytoTune®-iPS
センダイウイルスベクターを
利用した
iPS細胞作製法
センダイウイルスベクター
(SeVベクター)とは?
(SeVベクター)とは?
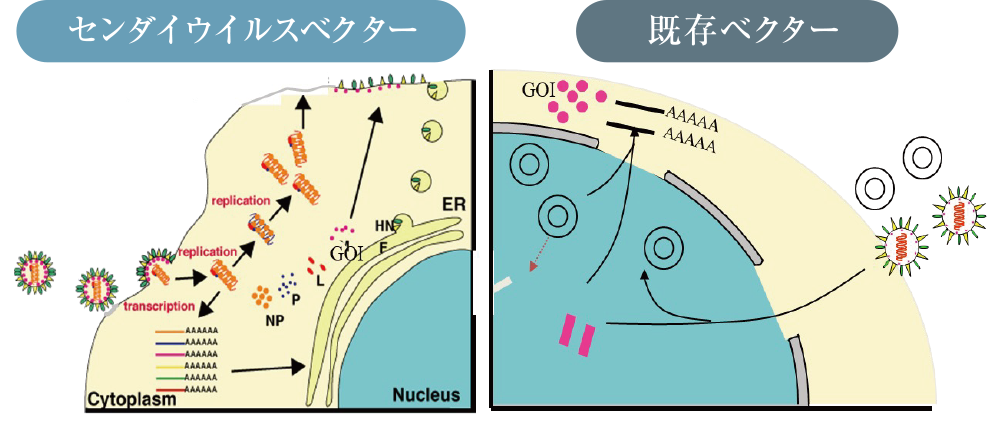
センダイウイルスベクターは核の中に入り込まずに運び込んだ遺伝子を核外細胞質内で働かせることができるため、原理上他のウイルスベクターで危惧される核内のゲノムを傷つける可能性はありません。また、IDファーマは細胞内からベクターを消失させる技術を開発しています。
Cyto Tune®-iPSはこのセンダイウイルスベクターを使用し、iPS細胞の作製に必要な遺伝子を細胞に送り届けます。「安全性」、「導入効率性」が高いという2つの特長を有しており、質の高いiPS細胞を作製することを可能にしたウイルスベクターの一つです。
既存のベクターの課題
- ○ 細胞の核の中に入り染色体を傷つけることから、癌化の可能性がある
▼
このような既存の課題を
センダイウイルスベクターはクリア
センダイウイルスベクターはクリア
- ○ 染色体を傷つけない
- ○ ベクターや初期因子が自然に消滅する
バンク事業に関わる準拠規制
当社は医薬品製造における、厳格な品質管理基準とされるGMP(Good Munufacturing Practics)に準拠した施設を持ち、取得する業許可を次に記載いたします。
- ① 特定細胞加工物製造業許可
- ② 再生医療等製品製造業許可
- ③ 医薬品製造業許可
(医薬品 生物学的製剤等) - ④ 医療機器製造業登録
この中で、i CELL BANKに関する業許可と準拠規制は下記の通りであり、関東信越厚生局より再生医療等の安全性の確保等に関する法律第35条第1項の規定により業許可を取得し、再生医療等の安全の確保等に関する法律に準拠した施設で製造を実施いたします。

つくば工場特定細胞加工施設で
取得する業許可
取得する業許可
特定細胞加工物製造業許可
準拠規制
<カルタヘナ法>
遺伝子組換え生物等の使用等の規制による生物の多様性の確保に関する法律
(平成15年法律第97号)
<再生医療等安全確保法>
遺再生医療等の安全性の確保等に関する法律
(平成二十五年法律第八十五号)
